
こんにちは!アルファゼミナールです。
化学の基本概念の一つである「モル」についてご存知でしょうか?モルは、物質の量を測るための単位であり、化学反応の計算や物質の特性を理解するために欠かせない重要な概念です。この記事では、モルの概念、その重要性、そして物質量を測る方法について詳しく解説します。
モルとは何か?

モル(mole)とは、物質の量を表す単位であり、国際単位系(SI単位系)において使用されます。1モルは、アボガドロ数(6.02214076 × 10²³個)の粒子(原子、分子、イオンなど)を含む量を指します。この数は、イタリアの科学者アメデオ・アボガドロにちなんで名付けられました。
例えば、水(H₂O)の1モルは、水分子が6.02214076 × 10²³個含まれていることを意味します。同様に、酸素(O₂)の1モルは、酸素分子が6.02214076 × 10²³個含まれていることを意味します。
モルの重要性
モルは、化学反応の計算や物質の特性を理解するために非常に重要です。以下に、その重要性をいくつかのポイントで説明します。
化学反応の計算: 化学反応式を使って、反応物と生成物の量を計算する際にモルが使われます。例えば、水の生成反応(2H₂ + O₂ → 2H₂O)では、水素と酸素のモル比を使って反応量を計算できます。これにより、反応の効率や収率を正確に評価することができます。
物質の特性の理解: 物質の特性(例えば、密度、圧力、体積など)は、モルを使って表現されることがあります。気体の法則(PV = nRT)では、物質量をモルで表現することで、気体の挙動を正確に予測することができます。
濃度の計算: 溶液の濃度をモル濃度(モル/L)で表現することが一般的です。これにより、溶液の性質や反応性を正確に評価することができます。例えば、1モル/Lの塩酸(HCl)溶液は、1リットルの溶液に1モルの塩酸が溶けていることを意味します。
物質量を測る方法
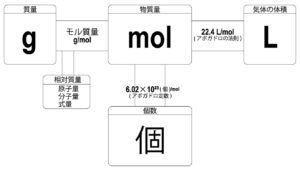
物質量を測る方法はいくつかありますが、以下に代表的な方法を紹介します。
モル質量を使った計算: モル質量(g/mol)は、1モルの物質の質量を表します。モル質量を使って、物質の質量からモル数を計算することができます。例えば、水(H₂O)のモル質量は約18g/molです。18gの水は、1モルの水分子を含んでいることになります。
式量と分子量の計算: 化学式からモル質量を計算する際には、各元素の原子量を使います。例えば、二酸化炭素(CO₂)のモル質量は、炭素(C)の原子量12と酸素(O)の原子量16を使って計算されます。具体的には、C(12) + 2O(16 × 2) = 44g/molとなります。
気体の体積を使った計算: 標準状態(STP: 0℃、1気圧)において、1モルの気体は22.4リットルの体積を持ちます。この性質を利用して、気体の体積からモル数を計算することができます。例えば、44.8リットルの二酸化炭素(CO₂)は、2モルのCO₂を含んでいることになります。
濃度を使った計算: 溶液の濃度を使って物質量を計算することもできます。モル濃度(M)は、溶液1リットル中に含まれる溶質のモル数を示します。例えば、1リットルの1モル/Lの塩酸(HCl)溶液には、1モルの塩酸が含まれています。
モルの概念を理解するための実例
実際の化学反応を例にとって、モルの概念をさらに深く理解してみましょう。
例1:メタンの燃焼反応: メタン(CH₄)が酸素(O₂)と反応して二酸化炭素(CO₂)と水(H₂O)を生成する反応を考えます。この反応は、次のように表されます。
CH₄ + 2O₂ → CO₂ + 2H₂O
ここで、メタン1モルと酸素2モルが反応して、二酸化炭素1モルと水2モルが生成されます。この反応式を使って、例えば10gのメタンが完全燃焼するのに必要な酸素のモル数や生成される二酸化炭素のモル数を計算することができます。
例2:塩化ナトリウムの溶解: 塩化ナトリウム(NaCl)が水に溶けると、ナトリウムイオン(Na⁺)と塩化物イオン(Cl⁻)に分解されます。この溶解反応を使って、例えば5.85gの塩化ナトリウムを溶かした溶液のモル濃度を計算することができます。
NaCl → Na⁺ + Cl⁻
塩化ナトリウムのモル質量は約58.5g/molなので、5.85gのNaClは0.1モルに相当します。これを1リットルの水に溶かすと、0.1モル/LのNaCl溶液が得られます。
結論
モルの概念は、化学の基本を理解する上で欠かせない重要な要素です。モルを使うことで、化学反応の計算や物質の特性の理解が深まり、実験や応用の幅が広がります。モルの概念とその重要性をしっかりと理解し、物質量を正確に測る方法を身につけることで、化学の学習が一層充実したものになるでしょう。この記事を通じて、モルの概念を楽しく学びましょう。
FAQs
モルとは何ですか? モルは、物質の量を表す単位であり、1モルはアボガドロ数(6.02214076 × 10²³個)の粒子(原子、分子、イオンなど)を含む量を指します。
モルの重要性は何ですか? モルは、化学反応の計算や物質の特性の理解、濃度の計算などに使われ、化学において非常に重要な概念です。
物質量を測る方法にはどのようなものがありますか? モル質量を使った計算、式量と分子量の計算、気体の体積を使った計算、濃度を使った計算などがあります。
モル質量とは何ですか? モル質量は、1モルの物質の質量を表すもので、単位はg/molです。化学式から各元素の原子量を使って計算します。
気体の体積を使ってモル数を計算する方法は? 標準状態(STP: 0℃、1気圧)において、1モルの気体は22.4リットルの体積を持ちます。この性質を利用して、気体の体積からモル数を計算できます。
この記事を書いた人
アルファゼミナール K.T